生体分子機能設計学研究分野 研究室のサイト
| 准教授 | 奥田 綾 | okuda.aya.5r*kyoto-u.ac.jp |
|---|---|---|
| 助教 | 黒川 南 | kurokawa.minami.2x*kyoto-u.ac.jp |
※メールアドレスは * を @ に置き換えてください
当研究室では生体高分子であるタンパク質の機能と構造の解明を通じて、多様な生命現象の分子機構の理解を目指している。さらに、タンパク質機能の改変・制御により、幅広い応用展開にも取り組んでいる。
- 酸化的フォールディング酵素の機能・構造研究
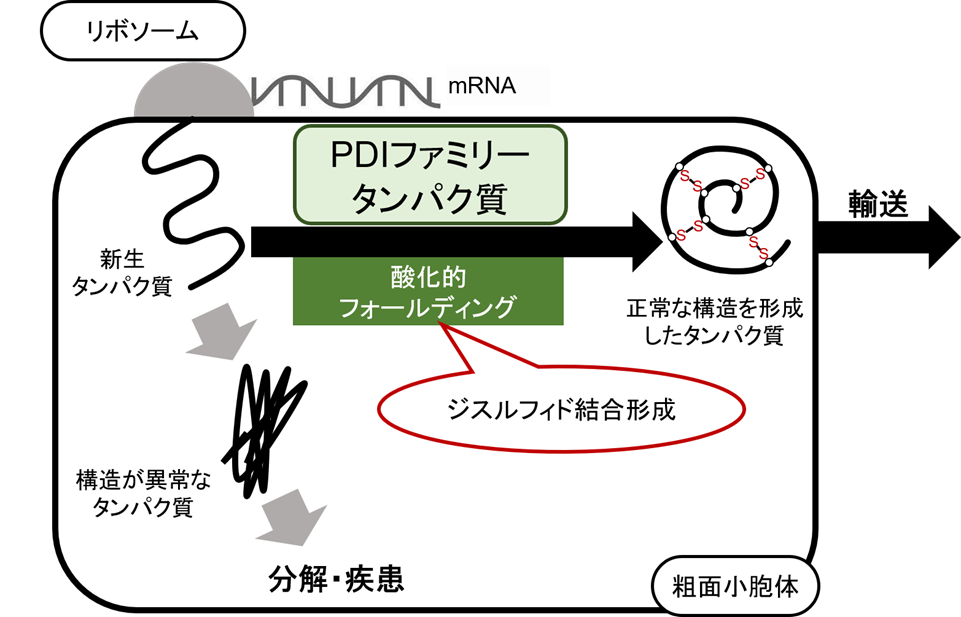
真核生物が生命機能を維持する上で重要な役割を果たす分泌タンパク質は、粗面小胞体上のリボソームで生合成される。リボソームがmRNAの遺伝情報を読み取り、新生タンパク質を小胞体内腔に送り込む。この新生タンパク質は、折りたたまれて正常な立体構造を形成すると輸送され、各所でその機能を発揮する。しかし、正しく立体構造を形成できなかったタンパク質は小胞体の品質管理機構によって分解されるか、蓄積して神経変性疾患等の原因となる。したがって、生命機能に重要なタンパク質が正しく輸送され機能するには、タンパク質の構造が正しく形成されることが不可欠であり、小胞体での立体構造形成機構の解明が求められている。
小胞体で生合成されるタンパク質の立体構造形成の多くはジスルフィド結合の形成を伴っている。これを酸化的フォールディングと呼び、この過程は酸化的フォールディング酵素群、Protein Disulfide Isomerase (PDI)ファミリータンパク質によって担われる。当研究室では、ヒトやダイズのPDIファミリータンパク質について、生化学的解析やX線および中性子の溶液散乱法を用いた構造解析により、その機能と構造を解析することで、酸化的フォールディングのメカニズムを解明する研究を進めている。
- タンパク質ライゲーションの技術開発
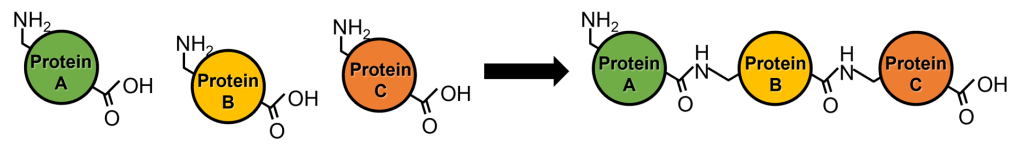
タンパク質のライゲーション技術とは、2つ以上のポリペプチドやタンパク質をペプチド結合などで人工的に繋ぎ合わせる技術である。通常、リボソームにおいてタンパク質が合成される際はアミノ酸が順次ペプチド結合によりN末端側から順番に繋ぎ合わされることで、タンパク質の全長が合成される。一方で、タンパク質ライゲーションではすでに合成が完了したタンパク質を繋ぎ合わせる。
本技術により、安定同位体修飾で特定のアミノ酸配列やドメインに着目したNMRや中性子小角散乱法による構造解析に加え、蛍光プローブ、非天然アミノ酸などの様々な生化学的・生物物理学的プローブをタンパク質に組み込むことが可能となる。さらに、ペプチドやタンパク質の環状化、全長では毒性を持つようなタンパク質の生産など、ペプチドおよびタンパク質工学へと展開が期待される。
しかしながら、タンパク質ライゲーションを高効率で安定して行うためには依然として課題が多く、それらを克服することで幅広いタンパク質に対して高い汎用性と自由度でライゲーションを可能にすることを目指し、技術開発を行っている。